https://closedi.jp/medical_supply#j_kyoukyu

姉妹サイトであるCloseDiにおいて【医薬品供給状況を検索ツール】を公開しています。供給状況データベース。このデータは厚生労働省のデータベース更新から1時間以内に反映されます。
https://closedi.jp/medical_supply#j_kyoukyu

姉妹サイトであるCloseDiにおいて【医薬品供給状況を検索ツール】を公開しています。供給状況データベース。このデータは厚生労働省のデータベース更新から1時間以内に反映されます。
姉妹サイトであるCloseDiにおいて【選定療養の対象となる医薬品の検索ツール】https://closedi.jp/medical_supply/#j_senteiryouyou を公開しています。
選定療養の対象となる医薬品の検索と増加額が計算できます。

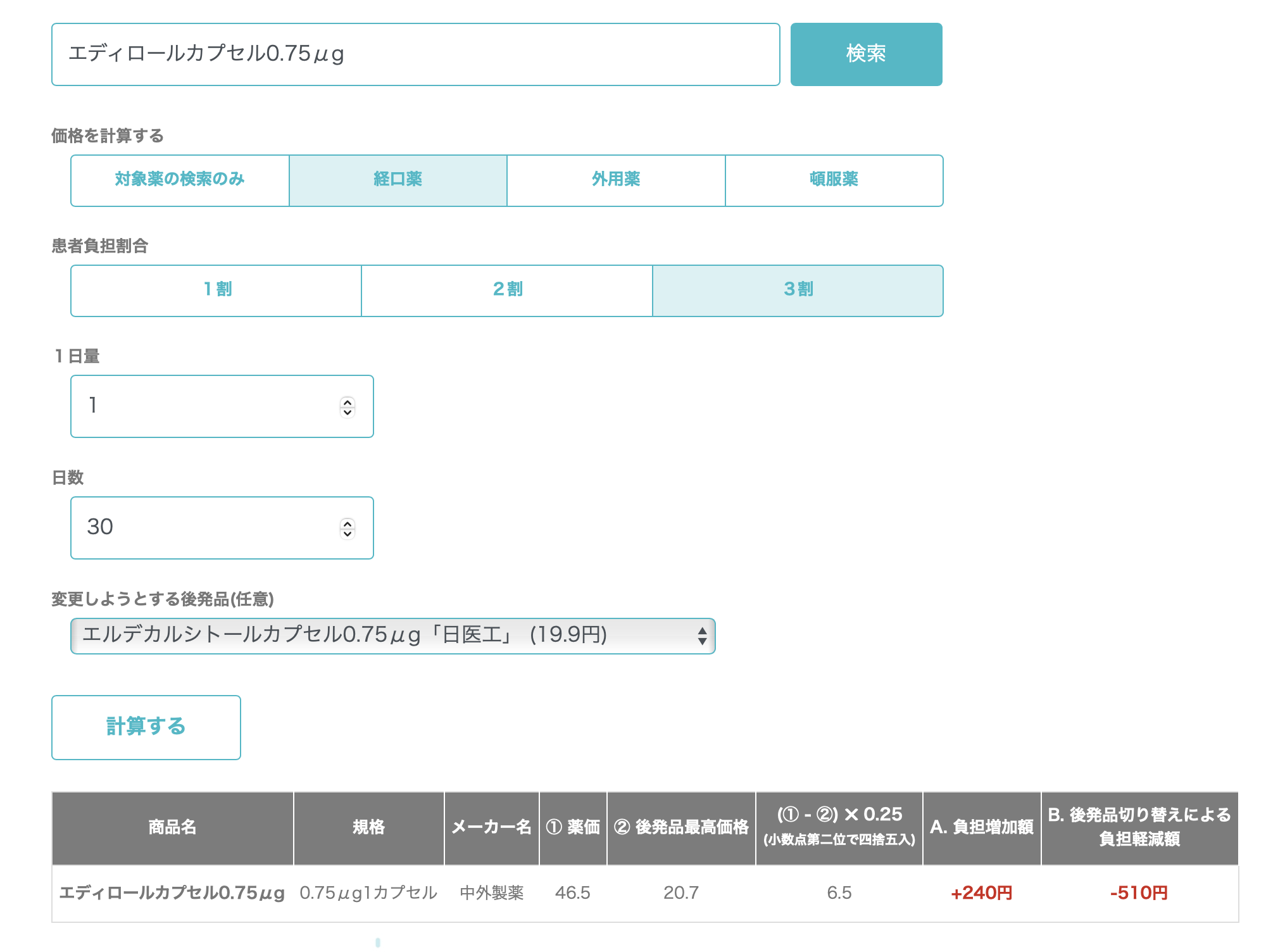
https://closedi.jp/medical_supply/#j_senteiryouyou
患者さんに説明する際に、ぜひご活用してください。
2024年12月に薬価収載される予定の新規成分の後発品が厚生省から公表されました。
2024年12月5日(金)に発売されます。(2024年12月更新)
経口剤
外用剤
注射剤
【A】トルカプ錠160mg, 200mgは新医薬品の処方日数制限により2025年5月末日までは1回14日分が限度である。2025年6月1日から長期投与可能である。
本剤は新医薬品であるため、厚生労働省告示第107号(平成18年3月6日付)に基づき、2025年5月末日まで、投薬期間は1回14日分を限度とされています。(添付文書より)
効果・効能
内分泌療法後に増悪したPIK3CA、AKT1又はPTEN遺伝子変異を有するホルモン受容体陽性かつHER2陰性の手術不能又は再発乳癌
シスタドロップス点眼液0.38%の新薬処方日数の投与制限は?は新医薬品の処方日数制限により2025年5月末日までは1回14日分が限度である。2025年6月1日から長期投与可能である。
本剤は新医薬品であるため、厚生労働省告示第107号(平成18年3月6日付)に基づき、2025年5月末日までは、投薬は1回14日分を限度とされている。(添付文書より)
効能又は効果
シスチン症における角膜シスチン結晶の減少
ボイデヤ錠50mgは新医薬品の処方日数制限により2025年4月末日までは1回14日分が限度である。2025年5月1日から長期投与可能である。
保険給付上の注意
本剤は新医薬品であるため、厚生労働省告示第107号(平成18年3月6日付)に基づき、2025年4月末日までは、投薬は1回14日分を限度とされている。
発作性夜間ヘモグロビン尿症
本剤は新医薬品であるため、厚生労働省告示第107号(平成18年3月6日付)に基づき、2025年4月末日までは、投薬は1回14日分を限度とされています。(添付文書より)
〈ターゼナカプセル0.1mg〉 BRCA遺伝子変異陽性の遠隔転移を有する去勢抵抗性前立腺癌 〈ターゼナカプセル0.25mg〉 BRCA遺伝子変異陽性の遠隔転移を有する去勢抵抗性前立腺癌 がん化学療法歴のあるBRCA遺伝子変異陽性かつHER2陰性の手術不能又は再発乳癌 〈ターゼナカプセル1mg〉 がん化学療法歴のあるBRCA遺伝子変異陽性かつHER2陰性の手術不能又は再発乳癌
以下に掲げる事務連絡については、令和6年4月1日付けで廃止すること。ただし、⑤から⑦までの事務連絡に関し、薬局開設者が令和6年3月31日以前に購入した医療用抗原検査キットについては、令和7年3月31日までの間、引き続き当該事務連絡の例により取り扱うことができること。 ① 「新型コロナウイルス感染症の拡大に際しての電話や情報通信機器を用いた診療等の時限的・特例的な取扱いについて」(令和2年4月10日付け厚生労働省医政局医事課、医薬・生活衛生局総務課事務連絡) ② 「歯科診療における新型コロナウイルス感染症の拡大に際しての電話や情報通信機器を用いた診療等の時限的・特例的な取扱いについて」(令和2年4月24日付け厚生労働省医政局歯科保健課、医薬・生活衛生局総務課事務連絡) ③ 「新型コロナウイルス感染症の拡大に際しての電話や情報通信機器を用いた診療等の時限的・特例的な取扱いに関するQ&A」(令和2年5月1日付け厚生労働省医政局医事課、医薬・生活衛生局総務課事務連絡(令和4年9月30日最終改正)) ④ 「新型コロナウイルス感染症の拡大を受けた薬局及び医薬品の販売業に係る取扱いについて」(令和2年4月24日付け厚生労働省医薬・生活衛生局総務課事務連絡) ⑤ 「新型コロナウイルス感染症流行下における薬局での医療用抗原検査キットの取扱いについて」(令和3年9月27日付け厚生労働省新型コロナウイルス感染症対策推進本部、医薬・生活衛生局総務課連名事務連絡(令和4年3月17日一部改正)) ⑥ 「新型コロナウイルス感染症流行下における薬局での医療用抗原定性検査キットの取扱いに関する留意事項について」(令和3年11月19日付け厚生労働省新型コロナウイルス感染症対策推進本部、医薬・生活衛生局総務課、監視指導・麻薬対策課連名事務連絡) ⑦ 「新型コロナウイルス感染症及び季節性インフルエンザ同時期流行下における薬局での医療用抗原定性検査キットの取扱いについて」(令和4年12月9日付け厚生労働省新型コロナウイルス感染症対策推進本部、医薬・生活衛生局総務課、監視指導・麻薬対策課連名事務連絡) ⑧ 「新型コロナウイルス感染症・季節性インフルエンザ同時期流行下における新型コロナウイルスに係る抗原定性検査キットの販売対応の強化について」(令和4年12月27日付け厚生労働省新型コロナウイルス感染症対策推進本部・医薬・生活衛生局総務課連名事務連絡) ⑨ 「抗原簡易キットの販売先について」(令和3年6月28日付け厚生労働省医薬・生活衛生局総務課事務連絡) ⑩ 「抗原簡易キットの販売先について(その2)」(令和3年10月15日付け厚生労働省医薬・生活衛生局総務課事務連絡) ⑪ 「抗原簡易キットの販売先について(その3)」(令和3年11月19日付け厚生労働省医薬・生活衛生局総務課事務連絡) ⑫ 「抗原簡易キットの販売先について(その4)」(令和4年1月14日付け厚生労働省医薬・生活衛生局総務課事務連絡) ⑬ 「抗原簡易キットの販売先について(その5)」(令和4年1月27日付け厚生労働省医薬・生活衛生局総務課事務連絡) (新型コロナウイルスの感染拡大に伴う薬局及び医薬品販売業に係る特例的措置関係事務連絡の廃止について 令和6年3月25日 厚生労働省医薬局総務課)
スチックゼノールAとフェルビナクスチック軟膏の主な違いは以下の通りです。
1. 外観が非常に似ているが、使用方法や有効成分、適応症に違いがある。
2. スチックゼノールAは底部を押して薬を出し、鎮痛・鎮痒成分を含むため虫刺されにも効果があるが、メントールの臭いがある
3. フェルビナクスチックは底部がネジ式で使いやすく、NSAIDs(非ステロイド性抗炎症薬)のフェルビナクのみを含むため、臭いが少ないとされている
使い分けのポイントは、以下の点を考慮することです。
・痛みと痒みの有無
・臭いの好み
・使いやすさ
フェルビナクスチックは、スチックゼノールと比較して、においがないことが人気の理由の一つと考えられます。
フェルビナクスチック軟膏3%「三笠」
下記疾患並びに症状の鎮痛・消炎
変形性関節症、筋・筋膜性腰痛症、肩関節周囲炎、腱・腱鞘炎、 腱周囲炎、上腕骨上顆炎(テニス肘等)、筋肉痛、外傷後の腫 脹・疼痛スチックゼノールA
下記における鎮痛・消炎
打撲、捻挫、筋肉痛、関節痛、骨折痛、虫さされ(各社添付文書より引用)
Rp.アポハイドローション 4.32g 1日1回 就寝前 両手掌に塗布
アポハイドローションは、処方箋上ではグラム(g)単位で処方する必要があるが、製品の包装にはミリリットル(mL)表記しかされていないという問題があった。この処方単位と包装単位の不一致により、薬局での調剤において混乱が生じていた
例えば、医師が「アポハイドローション4.32g」と処方した場合、薬剤師は包装のmL表記を見ながらグラム単位に換算しなければならなかった。この作業は手間がかかるだけでなく、計算ミスのリスクも伴う。
アポハイドローションの製造販売元である製薬会社が、包装単位をグラム表記に変更することを決定した。これにより、処方箋と製品の単位が統一され、薬局での調剤がより正確かつ効率的になることが期待された。