【コメント】
厚生労働省は2018年2月2日にゾフルーザ錠の製造販売を承認した。2018年5月に薬価収載予定である。
A型およびB型インフルエンザウイルスのキャップ依存性エンドヌクレアーゼ活性を選択的に阻害し、ウイルスmRNAの合成を阻害することにより、ウイルス増殖抑制作用を発揮する。既存のノイラミニダーゼ阻害薬とは異なった作用機序である。
以下に詳細を示す。(2018年2月25日時点)
参考 : ゾフルーザ錠 添付文書 第1版 https://www.shionogi.co.jp/med/download.php?h=383bb61b9f07173130c17c1848899a4a
ゾフルーザ錠 インタビューフォーム 第1版 https://www.shionogi.co.jp/med/download.php?h=1fdd914c8583f58b143be6cb133e6cb7
1. 規格はゾフルーザ錠10mgと20mgの2種類。
2. 適応は「A型又はB型インフルエンザウイルス感染症」
3. 予防投与は不可 (発売時点)
4. 用法用量
成人および12歳以上の小児は20mg錠2錠を単回経口投与する。
ただし、体重80kg以上の患者には20mg錠4錠を単回経口投与する。
12歳未満小児
40kg以上‥20mg錠2錠
20kg以上40kg未満‥20mg錠1錠
10kg以上20kg未満‥10mg錠1錠
5. 小児患者対象第Ⅲ相臨床試験では対象年齢は1歳から11歳までの患児に行なっている。
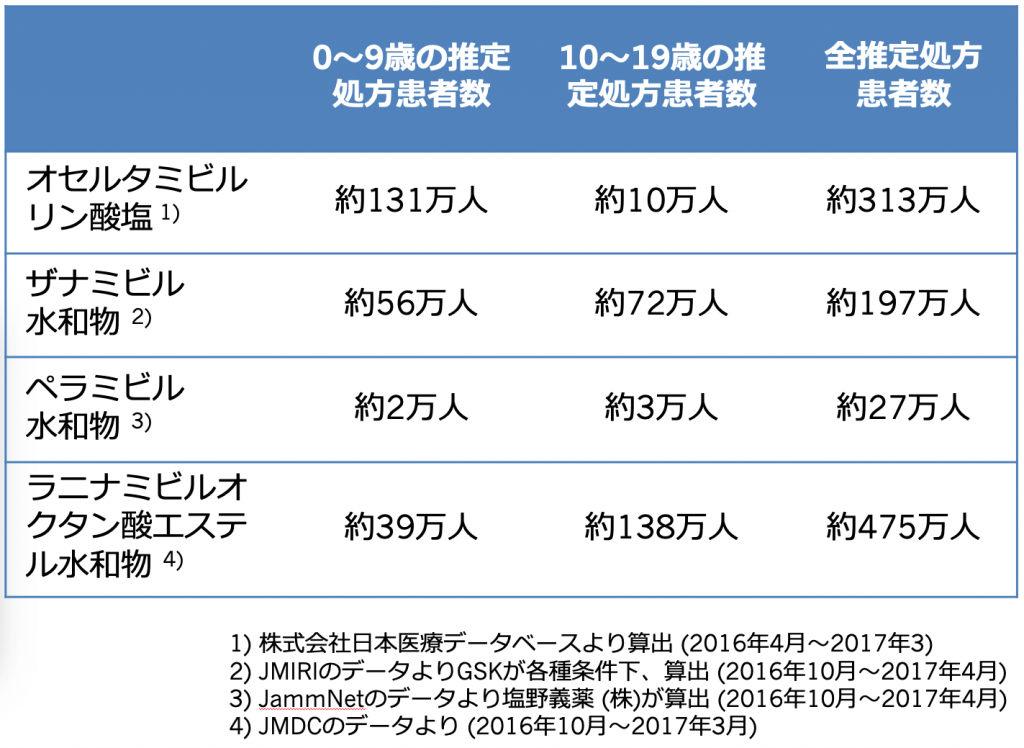
ゾフルーザ錠10mgの大きさは直径2.65mmと大きくはないが、1歳の患児に錠剤は飲めたのかという疑問は残る。1歳の患児に飲めたのであれば、イナビル吸入剤やタミフルドライシロップからゾフルーザ錠に大幅に切り替わっていくと考えられる。以下に2016年/2017年シーズンの国内での抗インフルエンザウイルス剤使用患者数を示す。
「0〜9歳」のタミフルドライシロップと「10〜19歳」のイナビル吸入剤がゾフルーザ錠に切り替われば相当の数になると思われる。
|
0〜9歳の推定処方患者数 |
10〜19歳の推定処方患者数 |
全推定処方患者数 |
| タミフル
(オセルタミビルリン酸塩 1)) |
約131万人
|
約10万人 |
約313万人 |
| リレンザ
(ザナミビル水和物 2)) |
約56万人
|
約72万人 |
約197万人 |
|
ラピアクタ
(ペラミビル水和物 3))
|
約2万人 |
約3万人 |
約27万人
|
| イナビル (ラニナミビルオクタン酸エステル水和物 4)) |
約39万人 |
約138万人 |
約475万人
|
1) 株式会社日本医療データベースより算出 (2016年4月〜2017年3)
2) JMIRIのデータよりGSKが各種条件下、算出 (2016年10月〜2017年4月)
3) JammNetのデータより塩野義薬 (株)が算出 (2016年10月〜2017年4月)
4) JMDCのデータより (2016年10月〜2017年3月)